1、人类卵母细胞成熟障碍的遗传机制研究
人类卵母细胞通过生发泡破裂、纺锤体组装、第一极体排出等一系列分子事件,经过GV期,MI期,发育为成熟的MII期卵子。只有高质量成熟的卵子才能与精子正常结合受精、启动后续胚胎发育并成功妊娠。临床辅助生殖中有相当部分患者卵子质量低下,表现为不能成熟、形态异常或退化等,导致辅助生殖反复失败。这一疾病的遗传原因及机制之前一直未知。团队相继发现了此过程异常的三种新孟德尔遗传病(卵子GV阻滞、MI阻滞、卵子死亡),鉴定出系列致病基因TUBB8 (NEJM, 2016);PATL2 (AJHG, 2017);WEE2 (AJHG, 2018);PANX1(Sci Transl Med, 2019);TRIP13 (AJHG, 2020);LHX8 (Genet Med, 2022);PABPC1L (EMBO Mol Med, 2023);COX15 (Proc Natl Acad Sci U S A, 2024)等,明确了致病机制并探索了干预策略。但这些基因只能解释少部分患者的病因,仍有大量患者病因未知,团队将开展系统深入探索。
2、人类早期胚胎停育的遗传机制研究
试管婴儿的大致过程为获取成熟卵子,而后于体外授精及胚胎培养,将正常发育到第3天或第5天的胚胎移植回患者子宫进行助孕。临床有相当部分不孕患者反复失败,表现为:胚胎在发育第3天停滞于8细胞之前,甚至伴有碎片化,即早期胚胎停育。此表型的遗传学原因所知甚少,团队前期发现了致此表型出现的多个突变基因PADI6 (AJHG, 2017);BTG4 (AJHG, 2020), CDC20 (Protein Cell, 2020);KPNA7 (J Clin Invest, 2023);TUBA4A (Genome Biol, 2023)等, 并揭示了致病机制。由于系列致病基因的发现,团队受邀在Science发表综述(Science,2023)。但是这些基因仅能解释少部分患者的遗传原因,团队拟深入揭示导致此表型出现的遗传机制。
3、卵母细胞成熟及早期胚胎发育的生理机制研究
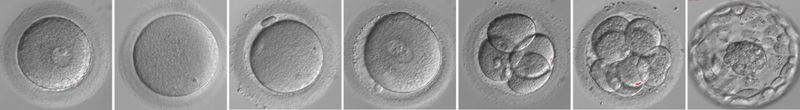
利用临床废弃的人GV卵母细胞及小鼠卵母细胞为模型,围绕生发泡破裂、纺锤体组装及染色体分离等关键事件,探索卵母细胞成熟及早期胚胎发育过程的分子机制,解析调控上述过程的新基因及新信号通路,尤其针对目前机制大都未知的人卵母细胞成熟过程。团队前期解析了人卵母细胞纺锤体启动组装及纺锤体双极化的独特机制(Science, 2022; Science, 2024),并阐释了人卵母细胞高比例非整倍体的发生机制(Cell Discov, 2023)。未来团队将利用人卵母细胞体外培养及删除小鼠等模型,结合高分辨率动态成像方法,深入探索卵母细胞成熟及早期胚胎发育的生理机制。
©复旦大学生殖与遗传团队 All rights reserved.

 English
English